Cáncer de hígado: avances en biología, tratamientos e inmunoterapia personalizada
El cáncer de hígado se ha consolidado como uno de los tumores más complejos y con peor pronóstico a nivel mundial, pese a los avances de las últimas décadas. En España y en el resto de Europa, los especialistas alertan de que sigue siendo una causa importante de mortalidad, con un peso creciente de factores de riesgo ligados al estilo de vida, como la obesidad, la diabetes o el consumo de alcohol.
Al mismo tiempo, la investigación traslacional y los nuevos enfoques de inmunoterapia y medicina de precisión están cambiando el panorama terapéutico. Centros de referencia como el Hospital Clínic de Barcelona, el IDIBAPS, la Clínica Universidad de Navarra y redes como el CIBEREHD lideran trabajos que van desde la comprensión de las bases biológicas del tumor hasta el diseño de vacunas personalizadas y estrategias de prevención poblacional.
Un tumor frecuente, letal y en crecimiento en todo el mundo
El cáncer hepático primario, donde el carcinoma hepatocelular (CHC o HCC) es la forma predominante, se sitúa entre los tumores más diagnosticados y es ya la tercera causa de muerte por cáncer a escala global. Se estima que alrededor del 80-85 % de los casos corresponden a carcinoma hepatocelular, mientras que aproximadamente un 10 % se deben a colangiocarcinoma intrahepático (iCCA), otra variante agresiva que se origina en los conductos biliares dentro del hígado.
En 2022 se notificaron cerca de 870.000 nuevos diagnósticos de cáncer de hígado en el mundo, y las proyecciones internacionales apuntan a que, si nada cambia, podrían superarse los 1,5 millones de casos anuales antes de 2050. Aunque las tasas ajustadas por edad pueden mostrar ligeros descensos gracias a las campañas de vacunación y a ciertos avances terapéuticos, el envejecimiento poblacional y la expansión de factores de riesgo metabólicos apuntan a un aumento absoluto de casos.
Este tumor se diagnostica a menudo en fases ya avanzadas, cuando las opciones de tratamiento potencialmente curativas (resección quirúrgica, trasplante hepático o ablación local) son muy limitadas. Por ello, las líneas actuales de trabajo se centran tanto en retrasar o evitar la aparición de la enfermedad como en mejorar la supervivencia de quienes ya la padecen, especialmente mediante fármacos sistémicos y procedimientos combinados.
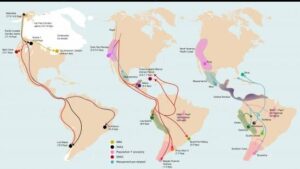
La carga del cáncer de hígado no se distribuye de forma homogénea. Estudios globales señalan que los países de renta baja y media soportan las tasas más altas de incidencia y mortalidad, en gran medida por un menor acceso a programas de cribado, a vacunas y a tratamientos antivirales o oncológicos. En regiones como Asia y parte de África, la infección por hepatitis B y la exposición a aflatoxinas alimentarias siguen teniendo un peso decisivo, mientras que en Europa gana importancia el componente metabólico.
Hallmarks del cáncer de hígado: cómo se comporta el tumor
En el marco del especial de la revista Cell dedicado a los 25 años del modelo conceptual «Hallmarks of cancer», un equipo del IDIBAPS y del Hospital Clínic de Barcelona ha coordinado una revisión exhaustiva sobre las bases biológicas del cáncer hepático. Bajo el título «Hallmarks of liver cancer: therapeutic implications», dirigido por el profesor Josep M. Llovet, se describen los procesos clave que permiten que las células del hígado se transformen en células cancerosas y se analizan sus consecuencias terapéuticas.
El trabajo subraya que el desarrollo del cáncer de hígado no depende de un único factor, sino de un conjunto de mecanismos biológicos que las células tumorales activan para crecer, evadir el control del organismo y adaptarse a un entorno hostil. Entre estos mecanismos se encuentran alteraciones en la proliferación celular, cambios en la forma de obtener energía y nutrientes, la capacidad de escapar del sistema inmunitario y la adaptación a contextos inflamados o fibróticos, como ocurre en el hígado cirrótico.
En el carcinoma hepatocelular, que suele surgir sobre un hígado dañado por cirrosis, destacan procesos como la proliferación descontrolada favorecida por mutaciones genéticas y por un microambiente inflamatorio crónico. También es clave la angiogénesis, es decir, la formación de nuevos vasos sanguíneos que nutren el tumor. Esta vía ha sido determinante para el desarrollo de fármacos antiangiogénicos que bloquean el eje VEGF, hoy pieza central de varios tratamientos sistémicos.
Otro rasgo fundamental es la capacidad del tumor para evitar la respuesta inmunitaria. Las células cancerosas pueden reducir la visibilidad de sus antígenos, expresan moléculas que inhiben la actividad de los linfocitos y modifican el entorno tumoral para hacerlo menos hostil. Esta comprensión ha impulsado el uso de combinaciones de inmunoterapia, como los inhibidores de puntos de control inmunitario, que tratan de reactivar las defensas del paciente frente al tumor.
En el colangiocarcinoma intrahepático, además de la angiogénesis y la evasión inmune, cobran especial relevancia las alteraciones metabólicas y ciertas mutaciones accionables. Entre ellas, se han identificado fusiones del gen FGFR2 y mutaciones en IDH1, ERBB2 o BRAF, entre otras. Aproximadamente en torno a la mitad de los iCCA muestran algún tipo de alteración para la que ya existe una terapia dirigida o se está investigando activamente, lo que abre la puerta a una medicina de precisión más afinada.
El conocimiento acumulado sobre la biología del cáncer de hígado ha impulsado una auténtica revolución terapéutica en las últimas dos décadas. En el carcinoma hepatocelular, el panorama ha pasado de contar con muy pocas opciones sistémicas para la enfermedad avanzada a disponer de varios fármacos dirigidos, combinaciones de inmunoterapia y estrategias secuenciales más complejas.
Entre los tratamientos actuales se incluyen antiangiogénicos que bloquean la formación de vasos sanguíneos del tumor, inhibidores de vías moleculares implicadas en el crecimiento y la supervivencia de las células malignas, así como combinaciones de inmunoterapia que se han consolidado como estándar en primera línea para muchos pacientes con enfermedad avanzada. Estos esquemas han logrado mejoras significativas en la supervivencia global y en la calidad de vida, aunque siguen sin ser curativos en la mayoría de casos.
En el colangiocarcinoma intrahepático, la medicina de precisión ha supuesto un punto de inflexión. La identificación de mutaciones accionables ha permitido introducir inhibidores específicos de FGFR2, terapias frente a IDH1 y otros fármacos dirigidos a alteraciones menos frecuentes pero con gran impacto individual. Paralelamente, la combinación de quimioterapia con inmunoterapia se ha convertido en una opción estándar para la enfermedad avanzada, buscando aprovechar tanto el efecto citotóxico clásico como la activación del sistema inmunitario.
Estos avances, como destaca el equipo del Clínic-Idibaps, son fruto directo de la investigación traslacional, que enlaza el hallazgo de mecanismos moleculares en el laboratorio con ensayos clínicos y cambios reales en la práctica asistencial. El artículo en Cell recoge a la vez el balance de 25 años de trabajo científico y las líneas futuras que podrían seguir mejorando el pronóstico del cáncer de hígado.
Buena parte de esta investigación cuenta con apoyo de programas internacionales, como el proyecto europeo THRIVE, que financia estudios centrados en identificar nuevas dianas terapéuticas y en optimizar el uso combinado de fármacos dirigidos, inmunoterapia y abordajes locorregionales en el contexto europeo.
Vacunas personalizadas para reforzar la inmunoterapia en cáncer de hígado avanzado
En paralelo a estos avances, uno de los campos más dinámicos es el de las vacunas personalizadas contra el cáncer. Investigadores del Cancer Center Clínica Universidad de Navarra y del Hospital Clínic de Barcelona están desarrollando una estrategia de vacunación destinada a potenciar la respuesta inmunitaria específica frente al cáncer de hígado en fases avanzadas, con la vista puesta en trasladar esta aproximación a pacientes alrededor de 2027.
El punto de partida es la constatación de que los inhibidores de puntos de control inmunitario (ICI), hoy pilar básico del tratamiento de muchos tumores hepáticos avanzados, solo logran respuesta en aproximadamente uno de cada tres o de cada cuatro pacientes. Los tumores que contienen un mayor número de linfocitos infiltrando el tejido tienen más probabilidades de responder a estos fármacos, por lo que el objetivo es aumentar de forma dirigida esa infiltración de células inmunitarias.
Para ello, los investigadores han empleado una herramienta de predicción de neoantígenos que ya habían utilizado en cáncer de mama y mieloma múltiple. A partir de muestras de tejido tumoral obtenidas en un ensayo clínico realizado en 2020, se secuenciaron los tumores de cada paciente y se identificaron mutaciones capaces de originar neoantígenos, es decir, nuevas proteínas que el sistema inmunitario puede reconocer como extrañas y contra las que podría lanzar una respuesta más intensa.
En modelos animales, el equipo del doctor Pablo Sarobe ha comprobado que, aunque el tumor muestra cierta respuesta espontánea frente a algunos de estos neoantígenos, su administración en forma de vacuna consigue multiplicar la intensidad de la respuesta inmune. Al vacunar con estos componentes, se observa un aumento notable de linfocitos específicos contra el tumor, lo que en teoría podría traducirse en mayor eficacia cuando se combinan con inmunoterapia estándar.
Sobre esta base, los científicos preparan un futuro ensayo clínico con pacientes de cáncer de hígado avanzado en el que se combinarán los ICI habituales con una vacuna personalizada de células dendríticas y neoantígenos. Esta aproximación busca entrenar al sistema inmunitario de cada persona con un «perfil» tumoral propio, de forma que pueda reconocer y atacar mejor las células malignas resistentes al tratamiento convencional.
Mecanismos moleculares: del splicing del ARN a nuevos biomarcadores
Otra línea de investigación emergente se centra en entender con mayor detalle qué ocurre dentro de las células tumorales hepáticas a nivel de expresión génica. Uno de los procesos que más interés está despertando es el llamado «splicing» del ARN, un mecanismo mediante el cual la célula recorta y recombina segmentos de sus transcritos de ARN para generar diferentes variantes de proteínas a partir de un mismo gen.
Proyectos actuales dedicados al carcinoma hepatocelular han observado que este proceso de splicing puede encontrarse alterado en las células cancerosas, dando lugar a moléculas anómalas que favorecen la progresión tumoral. En condiciones normales, la célula cuenta con sistemas de «control de calidad» que supervisan que el ARN se procese de manera adecuada, pero en el contexto del tumor hepático estos controles podrían fallar, permitiendo que se acumulen variantes perjudiciales.
El objetivo de estos estudios es determinar si esas alteraciones del splicing pueden convertirse en nuevos biomarcadores útiles para el diagnóstico precoz, la predicción de la evolución de la enfermedad o la selección más precisa de tratamientos. Para ello se están combinando técnicas de análisis genómico y transcriptómico en muestras de pacientes con modelos experimentales en cultivos celulares y en animales.
Si se confirman estas hipótesis, el splicing alterado del ARN podría convertirse no solo en una herramienta diagnóstica, sino también en una diana terapéutica en sí misma. Fármacos capaces de corregir o modular estos procesos, o de bloquear las variantes patológicas que generan, podrían sumarse en el futuro al arsenal contra el carcinoma hepatocelular, sobre todo en pacientes con tumores especialmente agresivos o resistentes a las terapias actuales.
Este tipo de investigación se enmarca en un movimiento más amplio hacia una oncología hepatológica más personalizada y basada en datos, en la que el perfil molecular del tumor de cada paciente oriente las decisiones terapéuticas y permita anticipar mejor tanto la respuesta como los posibles efectos adversos.
Factores de riesgo: del virus y el alcohol al hígado graso metabólico
Junto al desarrollo de nuevos tratamientos, los expertos insisten en que buena parte del esfuerzo debe dirigirse a reducir la aparición del cáncer de hígado. Diversas comisiones internacionales, como la publicada en la revista The Lancet, coinciden en que cerca del 60 % de los tumores hepáticos se asocian a causas prevenibles, lo que deja un margen considerable de actuación en salud pública.
Históricamente, los principales responsables han sido los virus de la hepatitis B y C, que continúan explicando en torno al 39 % de los cánceres de hígado. Aunque gracias a la vacunación frente a la hepatitis B y a los antivirales de acción directa frente al virus C se espera que este porcentaje se reduzca ligeramente en las próximas décadas, todavía queda trabajo por hacer, especialmente en la ampliación del cribado y el acceso al tratamiento.
En paralelo, está ganando terreno la enfermedad hepática esteatósica asociada a disfunción metabólica (conocida como MASLD o hígado graso de origen metabólico). Esta dolencia, que afecta ya a uno de cada tres adultos en muchos países, se relaciona con la obesidad, la resistencia a la insulina, la diabetes tipo 2, la mala alimentación y el sedentarismo. En sus formas más graves, puede evolucionar hacia inflamación intensa, fibrosis avanzada, cirrosis y, finalmente, cáncer de hígado.
El consumo de alcohol sigue siendo otro de los factores clave. Se calcula que alrededor del 19 % de los tumores hepáticos actuales están ligados al alcohol, porcentaje que podría aumentar si no se adoptan medidas adicionales. Los especialistas recuerdan que no existe un nivel de consumo completamente exento de riesgo y que hay personas que desarrollan hepatopatía y cáncer incluso con ingestas que podrían considerarse moderadas.
Además, en determinadas regiones del mundo continúan presentes riesgos ambientales como las aflatoxinas, toxinas producidas por hongos que pueden contaminar alimentos básicos y aumentar el riesgo de carcinoma hepatocelular, sobre todo cuando coinciden con infección por hepatitis B. Aunque en Europa los controles alimentarios han reducido mucho este problema, es un factor que sigue pesando en la carga global de la enfermedad y subraya la importancia de la seguridad alimentaria.
Prevención, cribado y retos para los sistemas sanitarios
Los investigadores coinciden en que, si se combinan políticas de prevención primaria con programas de detección temprana y un acceso más equitativo a los tratamientos, es posible reducir de manera sustancial la mortalidad por cáncer de hígado en los próximos años. En el caso de España y Europa, las recomendaciones pasan por reforzar varios frentes de manera coordinada.
En primer lugar, se subraya la necesidad de mantener y ampliar la vacunación contra la hepatitis B, así como garantizar el diagnóstico y tratamiento universales de la hepatitis C mediante estrategias de cribado poblacional. Varios expertos abogan por realizar al menos una prueba de detección de virus de la hepatitis a todas las personas adultas a lo largo de su vida, algo que podría implementarse aprovechando contactos habituales con el sistema sanitario.
En segundo lugar, se propone actuar de forma más decidida sobre el consumo de alcohol mediante campañas de concienciación, etiquetados claros, restricciones de marketing y medidas fiscales que desincentiven los consumos elevados. En paralelo, se recomienda promover estilos de vida saludables basados en la dieta mediterránea, la actividad física regular y el control del peso corporal, con especial atención a personas con síndrome metabólico o diabetes.
Respecto al hígado graso de origen metabólico, los especialistas recuerdan que, si el daño hepático aún no es profundo, la enfermedad puede revertirse con cambios de estilo de vida. La pérdida de peso, incluso de un 7-10 % en algunos casos, puede mejorar la inflamación y la fibrosis. Además, nuevos fármacos para la obesidad, como los agonistas del receptor GLP-1, están mostrando capacidad para reducir la inflamación hepática y frenar la progresión de la fibrosis, lo que podría tener un impacto relevante en la prevención del cáncer hepático a medio plazo.
Por último, es clave potenciar el cribado en población de riesgo. Las guías clínicas recomiendan realizar ecografías periódicas, habitualmente cada seis meses, a personas con cirrosis o con determinados factores de riesgo acumulados. Sin embargo, la realidad es que muchos casos todavía se detectan tarde. Mejorar la sensibilización de la población y de los profesionales sanitarios de atención primaria y digestivo es un paso imprescindible para elevar las tasas de diagnóstico en fases iniciales.
En conjunto, las evidencias científicas apuntan a que, aunque el número absoluto de casos de cáncer de hígado pueda seguir aumentando por razones demográficas y metabólicas, gran parte de esa carga es teóricamente evitable mediante estrategias bien coordinadas de prevención, detección precoz e innovación terapéutica. El reto para los sistemas sanitarios europeos será combinar estas piezas de manera eficiente y garantizar que los avances lleguen también a los colectivos más vulnerables.